Et le second principe de la thermodynamique ?
Ce blog s'enorgueillit de propager les bonnes manières, la langue française et le second principe de la thermodynamique. Hélas je n'ai pas réparti mes efforts de manière équitable entre ces trois grands thèmes. Qui trop embrasse mal étreint, et je ne sais comment font ceux qui affichent pour priorités à la fois l'éducation, la défense, la réduction des effectifs de l'administration, le maintien de la qualité du service public, la diminution de la dette et celle, simultanée, des charges affectant les entreprises.
 Mais passons. Pas plus tard qu'avant-hier soir, j'entendais dans le métro quelqu'un dire à son voisin (c'était sur la ligne reliant Clichy-sous-Bois et Sarcelles) :
Mais passons. Pas plus tard qu'avant-hier soir, j'entendais dans le métro quelqu'un dire à son voisin (c'était sur la ligne reliant Clichy-sous-Bois et Sarcelles) :
- Bel ami, voudriez-vous bien me donner l'heure, je vous prie ? Je dîne en ville ce soir et je crains fort d'être en retard. La duchesse de Guermantes est intraitable sur la ponctualité, vous le savez autant que moi, cher Mohamed.
- Il est sept heures moins le quart, très cher Khaled. Vous aurez tout le temps de passer votre smoking et de polir le madrigal que vous comptiez déclamer à cette chère Oriane entre le homard et le foie-gras truffé.
Cette conversation me remplit de fierté et de satisfaction lorsque je me rendis compte que toute allusion au second principe de la thermodynamique en était absente. Rien. Que dalle. Nada. Nothing. Nihil.
Il va falloir rattraper le retard à marche forcée... Voilà donc un petit cours sur le second principe de la thermodynamique.
Le second principe introduit la fonction d'état extensive S, appelée entropie. La variation d'entropie d'un système, lors d'une transformation quelconque, peut être décrite comme la somme d'un terme d'échange et d'un terme de création :
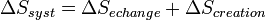
- Le terme de création, toujours positif ou nul, impose le sens de l'évolution de la transformation,
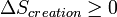 ; l'égalité n'a lieu que pour une transformation réversible.
; l'égalité n'a lieu que pour une transformation réversible. - Le terme d'échange dans le cas d'un système fermé échangeant la quantité de chaleur Q avec le milieu extérieur à la température T est égal à
 .
.
Une autre formulation est possible comme nous l'avons vu précédemment, en considérant l'entropie du système et l'entropie du milieu extérieur.
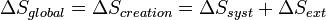
 La variation d'entropie globale correspond à l'entropie créée et est égale à la somme des variations d'entropie du système et du milieu extérieur. Elle est toujours positive dans le cas des transformations réelles irréversibles. En revanche dans le cas idéal des transformations réversibles elle est nulle.
La variation d'entropie globale correspond à l'entropie créée et est égale à la somme des variations d'entropie du système et du milieu extérieur. Elle est toujours positive dans le cas des transformations réelles irréversibles. En revanche dans le cas idéal des transformations réversibles elle est nulle.
Considérons une transformation effectuée soit de façon réversible soit de façon irréversible, à la température T. L'entropie étant une fonction d'état sa variation sera la même pour les deux chemins envisagés. En revanche la chaleur dépendra du chemin suivi car elle n'est pas une fonction d'état.
- Transformation réversible:
 puisque l'entropie créée est nulle.
puisque l'entropie créée est nulle.
- Transformation irréversible:
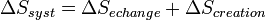
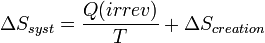
Il s'ensuit que  puisque l'entropie créée est positive.
puisque l'entropie créée est positive.
L'expression ainsi obtenue a été formulée par Clausius. On l'appelle encore inégalité de Clausius. C'est une autre façon d'exprimer le second principe.
Alors, ça vous plaît ? On continue demain ?
